除铁除锰常规水处理工艺介绍
2025-05-10 来自: 衡美水处理公众平台 浏览次数:256
衡美水处理为您介绍一项水处理专业知识——除铁除锰的常规水处理工艺介绍。
含铁、含锰的地下水在我国分布很广,铁和锰可以共存于地下水中,并常以溶解度较高的二价铁、二价锰形式存在。
水中富含的铁离子会使水发黄,有明显的铁锈气味,易使衣服和器皿着色发黄,还易促进管网中铁细菌的生长,对生活、生产用水造成污染,对管路造成损害。另外,铁含量高的水进入锅炉和换热设备,易结生氧化铁垢和垢下腐蚀;铁含量较高的原水进入离子交换器,易使树脂中毒。
锰是人体及动植物所需的微量元素之一,但摄入过量的锰会引起中毒,长期接触锰化合物也可造成锰中毒。含锰水会使水有色、臭、味,影响纺织、造纸、酿造、食品等工业产品质量,也会对家用器具造成污染,洗涤衣物会有微黑色或浅灰色的斑渍。
含铁锰的地下水暴露在空气中一段时间后,沉淀出棕黄色沉淀物
富含铁、锰离子的水对人类生活、工农业生产会造成较大危害,因此需要经过处理后方可使用。
一、除铁
地下水中的二价铁不稳定,常使用曝气法去除。地下水中二价铁盐通常以重碳酸铁Fe(HCO3)2的形式存在。一般是将地下水通过水泵抽入曝气池中,并在输水管路或曝气池中通入压缩空气或通过射流法在管路中混入空气,从而使空气中的氧气与水充分混合,达到将二价铁氧化成三价铁的目的;再通过锰砂或其他除锰滤料过滤,去除氧化铁沉淀物。
锰砂(主要成分是二氧化锰)是二价铁氧化成三价铁的良好催化剂。当pH值大于5.50时(一般应保持原水pH值为6.5-7.0可取得较好的处理效果),能加速二价铁氧化成三价铁的过程。其化学反应方程式如下:
4Fe2++O2+8OH-+2H2O → 4Fe(OH)3↓
氧化过程中,水中须保持足够的溶解氧,才能将二价铁氧化成三价铁,并在水解后呈胶体氢氧化铁以褐色絮状物沉淀,可经锰砂滤层过滤将铁除去。
二、除锰
氧化除锰基本与除铁一样,含锰水经曝气后经过锰砂滤料,在锰砂滤料表面的锰质活性滤膜作用下,Mn2+被溶解氧氧化为MnO2,吸附在滤料表面,使滤膜得到更新,该过程也是自催化反应。其反应式为:
2Mn2++O2+4OH- → 2MnO2↓+2H2O
水中的二价锰盐在过滤时,也可能因MnO吸附而发生下列化学反应:
MnO2 ·H2O+Mn2++2OH- → MnO2 ·MnO·H2O+H2O
注:MnO2 ·H2O指有效锰砂;MnO2 ·MnO·H2O指失效锰砂。
锰砂与Mn2+结合生成三氧化二锰后,便失去了除锰的性能。需要加入氧化剂再生。 使MnO2 ·MnO重新氧化成MnO2。一般生产中多采用往水中加氯(Cl2)的方法,来恢复锰砂的除锰性能。其反应式为:
MnO2 ·MnO·H2O+2H2O+Cl2 → 2MnO2 ·H2O+2HCl
锰的去除远比除铁困难,铁、锰共存时,铁对锰的去除有干扰。在滤层中,要先完成对铁的去除,才能开始除锰,因此要获得稳定的除锰效果,Fe2+的浓度不应超过2mg/L。
三、铁锰共存的去除方法
当原水中铁锰含量较高,含Fe量超过5mg/L、含锰量超过1.5mg/L时,若用锰砂同时进行处理,由于铁比锰易于氧化,二价锰较难被氧化为四价锰。因此,一般需要采用二次过滤法,即先除铁,使Fe2+的浓度低于2mg/L,再除锰。其流程为:地下水→深井泵(变频泵)→曝气→一 级过滤(除铁)→二级过滤(除锰)。
当原水中铁锰含量较低,含铁量低于5mg/L、含锰量低于1.5mg/L时,可以采用一次过滤去除。其流程为:地下水→深井泵(变频泵)→曝气→过滤(同时除铁除锰)。
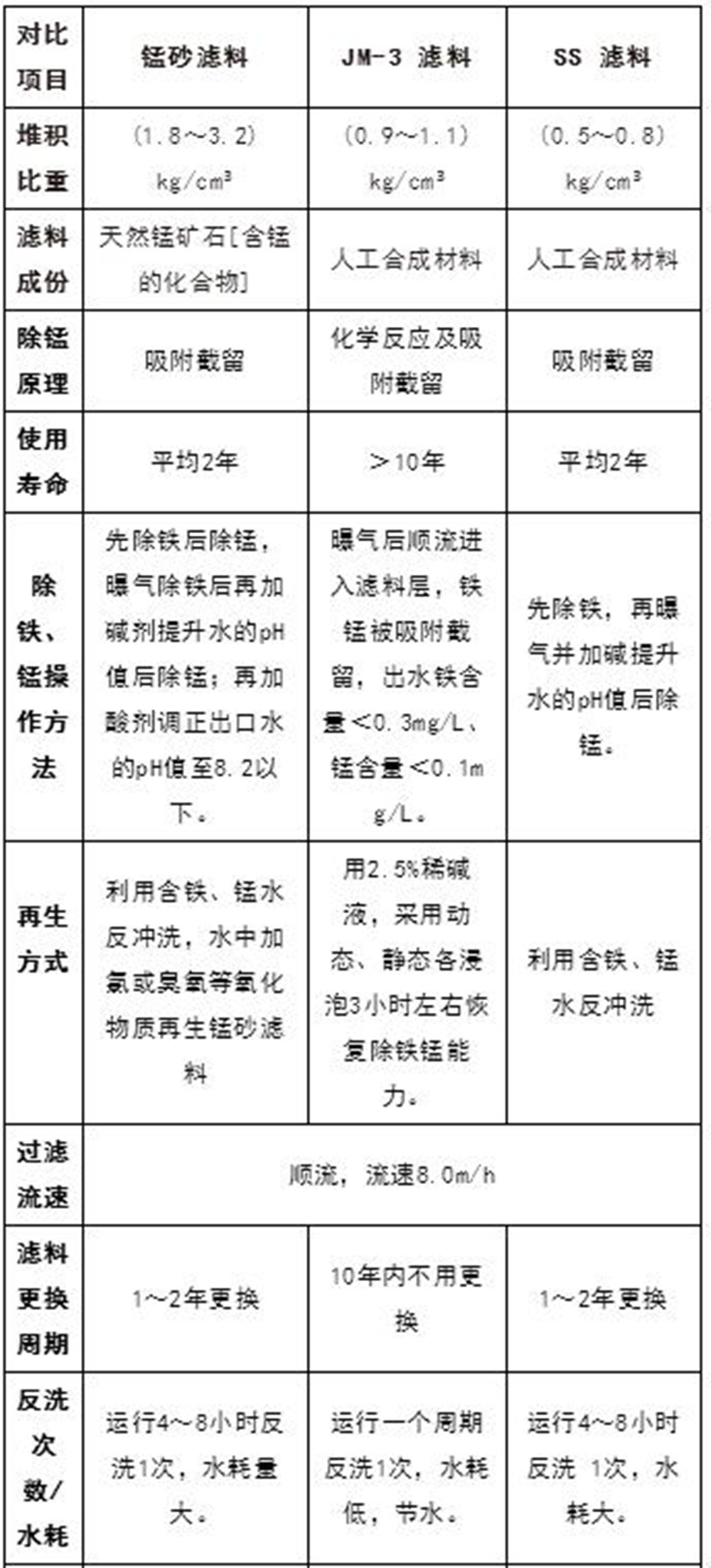
目前国内常用除铁锰的滤料有:锰砂、SS滤料、人工合成的分子筛“JM-3型”滤料,主要是采用化学反应和吸附截留的原理来实现。
锰砂主要是利用表面的锰质活性滤膜MnO2进行除锰;
SS滤料是一种含硅、铁、铝的多孔状颗粒滤料,具有良好的过滤、吸附和絮凝沉淀作用;
JM-3型滤料是一种硅、铝、氧的晶格状四面体,其采用吸附与离子交换两种方式去除。
JM-3除铁锰滤料中的硅与铝交换,而铝是三价、硅是四价,缺少一个电荷,需要正电荷的离子补充。当水与JM-3滤料接触时,水中带正电荷的离子可补充JM-3滤料中缺少的电荷,从而被滤料吸附,达到净水的目的。它可以有效地去除水中绝大部分无机盐类和部分有机物,去除率在70%~90%,特别是处理毒理学物质中的氟、砷、汞、铅、镉、硒、钼以及铁、锰、锌、钙、镁等,效果显著。

实现城市用水洁净处理,营造和谐人居生活环境。








